2025年4月,《NPJ Vaccines》期刊發表了一項重要研究,題為《Impact of inactivated vaccine on transmission and evolution of H9N2 avian influenza virus in chickens》。研究發現,H9N2禽流感病毒可通過一種獨特機制逃避免疫系統,從而對傳統滅活疫苗產生的宿主免疫實現“免疫逃逸”。該研究為我們深入理解H9N2病毒的傳播與進化路徑,以及現有疫苗防控策略的潛在局限性,提供了科學依據。
揭示H9N2滅活疫苗局限:雞上呼吸道病毒復制未受抑制,增加傳播風險
研究發現,接種H9N2禽流感滅活疫苗的3周齡SPF雞未能獲得有效保護,仍出現上呼吸道組織損傷,如鼻甲黏膜病變、喉充血(圖2)。免疫分析顯示,其上呼吸道局部IgG抗體水平僅為血清的3.65%(圖1),表明滅活疫苗誘導的局部體液免疫弱。這種免疫應答不足以中和呼吸道內高水平復制的病毒,導致病毒在免疫雞群中持續存在和傳播。更關鍵的是,在疫苗免疫壓力下,H9N2病毒快速發生適應性進化,積累關鍵突變(如HA變異),顯著增強了其復制和傳播能力,最終突破免疫屏障。
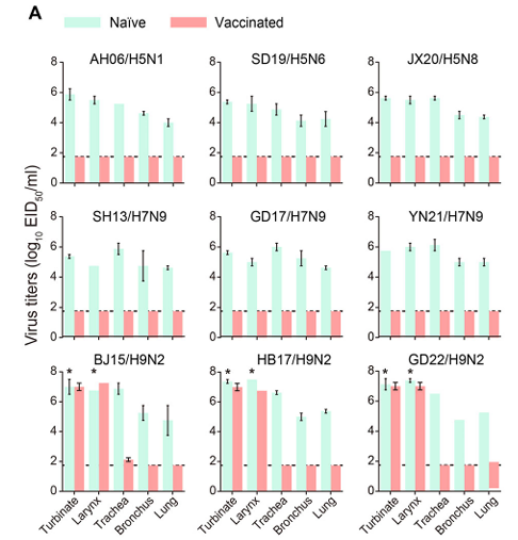
圖1. 不同流感亞型免疫攻毒組,不同器官病毒含量情況
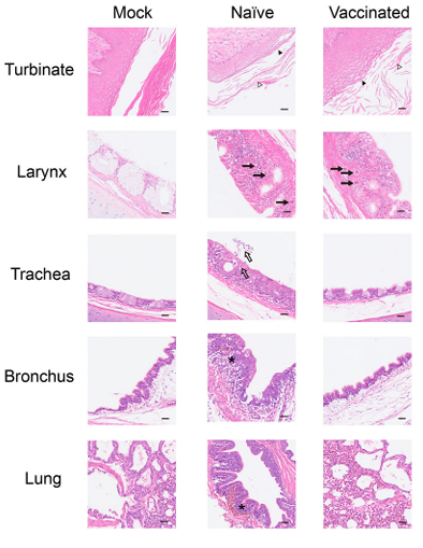
圖2.H9N2免疫攻毒組鼻甲和喉部的病理變化
黏膜免疫疫苗:阻斷H9N2禽流感傳播的關鍵策略
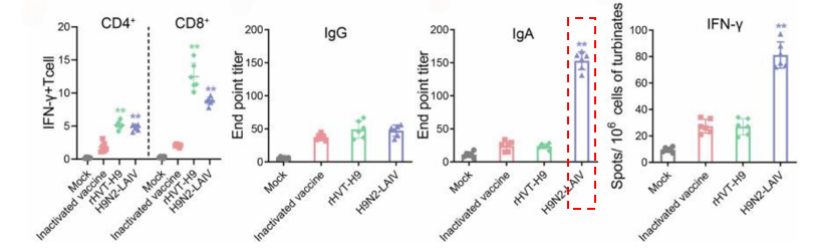
圖3.不同類型的H9N2疫苗免疫后細胞免疫和體液免疫變化情況
通過比較禽流感滅活疫苗(Inactivated vaccine)和減毒活疫苗H9N2-LAIV的效果發現, H9N2-LAIV 疫苗能誘導接種雞上呼吸道黏膜 IgA 顯著升高和鼻黏膜細胞IFN-γ表達增強(圖3)。這些數據表明,有效防控雞群H9N2禽流感病毒關鍵在于加強細胞免疫和上呼吸道黏膜免疫。
無獨有偶,中國農業科學院團隊在《Animal Diseases》期刊發表的一項研究也揭示了H9N2滅活疫苗面臨的重要挑戰:當母源抗體(HI滴度)達到6log2及以上時,會完全抑制疫苗的免疫效果。研究發現,1日齡商品雞接種滅活疫苗后,無法產生新的抗體應答,而母源抗體則會隨著雛雞生長逐漸衰減,造成一個“免疫空窗期”。在此期間,雞群對H9N2病毒高度易感(見圖4)。該研究進一步凸顯了研發可突破母源抗體干擾的新型疫苗策略的緊迫性和必要性。
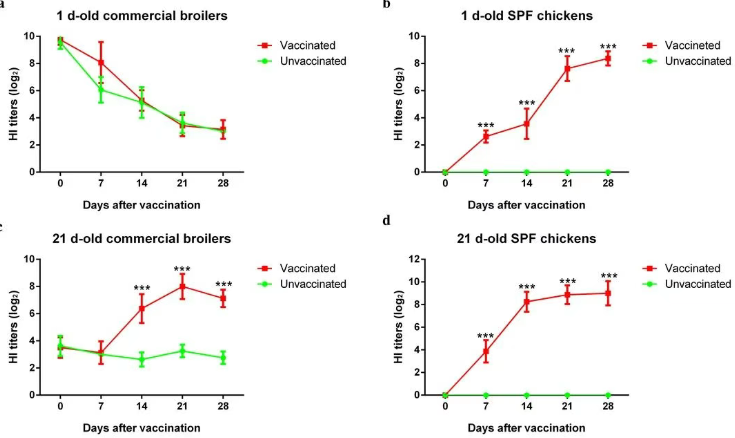
圖4.商品雞和SPF雞免疫H9N2亞型禽流感滅活疫苗后的抗體水平變化
不可缺少的黏膜免疫疫苗
雞體呼吸道、消化道黏膜的上皮和皮膚是機體內部和外界環境之間的屏障,其構成了免疫系統重要的第一道防線。黏膜是禽流感病毒感染的主要部位及黏膜免疫的發生部位。50%以上禽類病原經黏膜感染,黏膜免疫在機體抵御禽流感的入侵中發揮重要作用。
迪福潤絲生物全球首創的H9N2禽流感減毒黏膜免疫疫苗
迪福潤絲生物自主研發的H9N2禽流感減毒黏膜免疫疫苗可作用于黏膜系統,誘導機體局部黏膜免疫(SIgA為主),形成由體液-細胞-黏膜免疫組成的三重免疫防護。
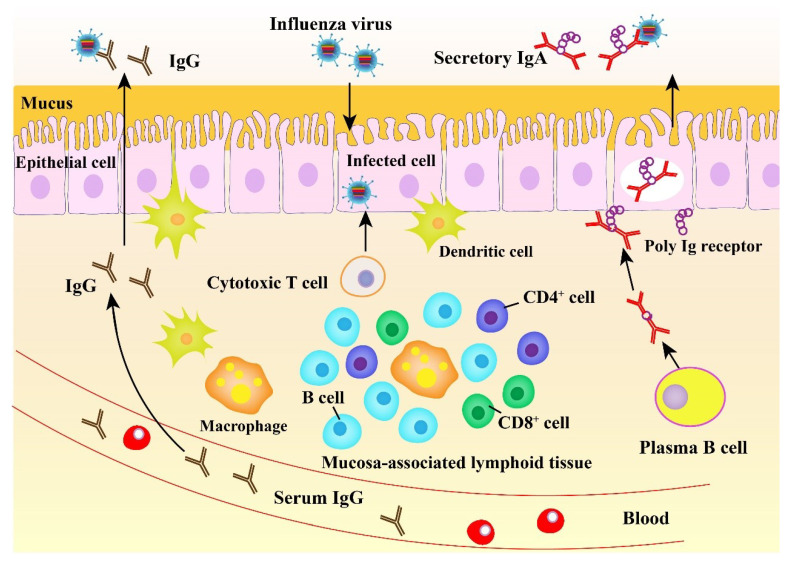
圖5.禽類黏膜免疫的作用機制
突破母源抗體干擾
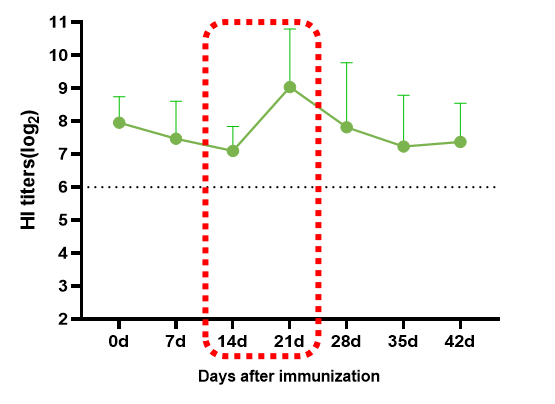
圖6.H9N2黏膜免疫疫苗田間試驗HI抗體檢測
在對3000只雞進行的田間試驗中,接種迪福潤絲生物H9N2黏膜免疫疫苗后,通過HI抗體檢測發現,該疫苗在免疫初期起效迅速,接種后42天內HI抗體水平始終維持在2?以上(圖6)。這一結果不僅有效填補了傳統油苗在免疫初期的“空白期”,更突破了母源抗體干擾所帶來的免疫抑制,為早期構建穩定、持久的免疫保護屏障提供了有力保障。
安全性更高:接種后幾乎不排毒
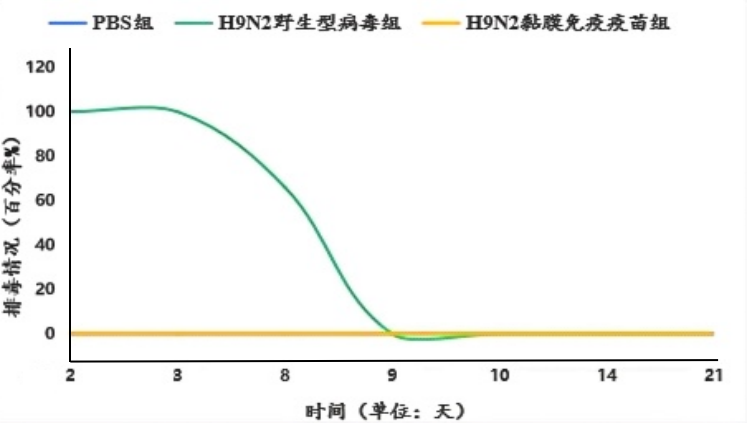
圖7. H9N2黏膜免疫疫苗體內減毒特征:感染SPF雞后排毒情況
在對SPF雞接種迪福潤絲生物H9N2黏膜免疫疫苗后,從第2天起對免疫后的SPF雞進行咽拭子、泄殖腔拭子的病毒排毒檢測。結果顯示,在連續3周的監測期內,均未檢出活病毒排出(圖7),表明該疫苗在阻斷病毒復制和切斷傳播鏈方面展現出良好的生物安全性與防控潛力。
疫苗保護效力更佳:可以誘導高水平HI抗體
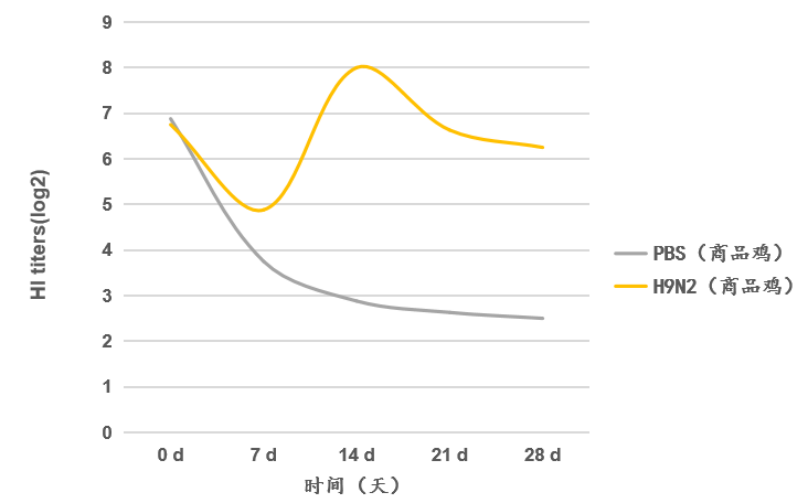
圖8. 2次免疫商品雞后HI抗體檢測水平
研究者在試驗中選取10日齡商品雞,采用滴鼻加點眼方式進行免疫接種,在第0天進行初次免疫,第7天進行加強免疫。隨后分別在第0、7、14、21和28天對雞群進行HI抗體檢測(圖8)。結果顯示,迪福潤絲生物H9N2黏膜免疫疫苗在完成兩次免疫后,可穩定誘導商品雞產生高水平HI抗體,抗體滴度持續維持在26以上,表明該疫苗具有良好的免疫原性。
迪福潤絲生物H9N2禽流感減毒黏膜免疫疫苗具有顯著的差異化優勢:
表1.迪福潤絲生物H9N2禽流感減毒黏膜免疫疫苗相比較于已上市或在研H9N2疫苗的優勢
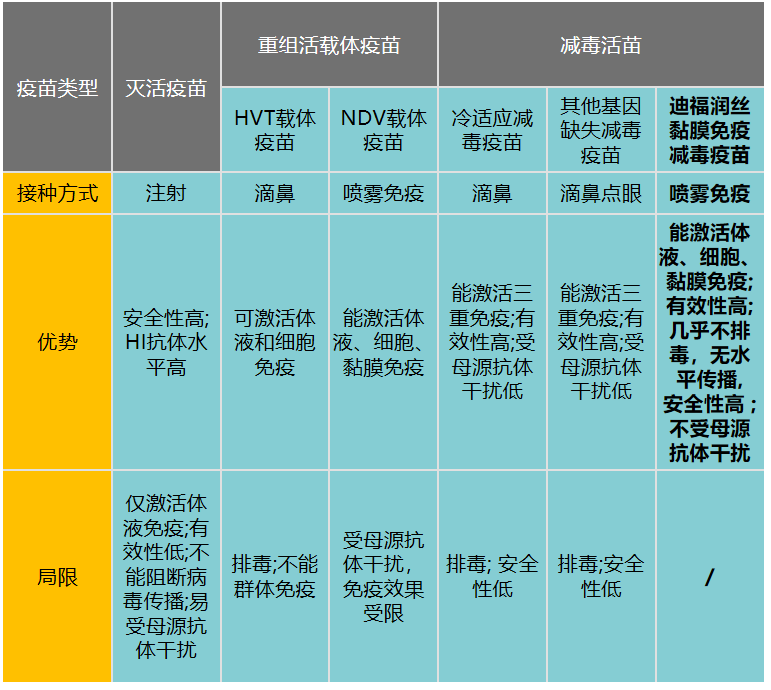
迪福潤絲生物H9N2減毒黏膜免疫疫苗不僅在免疫效果上實現躍升,更在實際應用中提供了解決母源抗體干擾、病毒傳播控制等“卡脖子”問題的創新路徑,以開創性實力重新定義H9N2禽流感防控,引領新一代疫苗變革!
參考文獻:
Hu Z , Ai H , Wang Z ,et al.Impact of inactivated vaccine on transmission and evolution of H9N2 avian influenza virus in chickens[J].NPJ Vaccines.2025.10(1).
Pan X., Su X., Ding P.Y., et al. Maternalderived antibodies hinder antibody response against H9N2 AIV inactivated vaccine in the field[J]. Animal Diseases. 2022.
