在上次的熒光選擇的軟文中,我們提到了一個研究蛋白互作的技術(shù)——生物發(fā)光共振能量轉(zhuǎn)移(BRET),這里我們再回顧一下這個技術(shù)最核心的幾個要點(diǎn):
1. 能量并不只是可以以光子躍遷的形式激發(fā),也可以以共振的形式傳遞給相鄰或者非常接近的可以接受能量的物質(zhì)中。
2. 熒光素酶本身不需要被光激發(fā),只需要添加底物即可通過生物酶促反應(yīng)產(chǎn)生光,這里螢火蟲熒光素酶的反應(yīng)是需要ATP參與的,但是RLuc和Nluc(nanoLuc)的底物酶促反應(yīng)是不需要ATP的參與。
3. 熒光素酶本身穿透力強(qiáng),即使是在機(jī)體的深層臟器發(fā)出的光,也可以被檢測到,且強(qiáng)度沒有受到較大影響。
回顧結(jié)束,今天我們來聊一聊這個體系的其他用途,除了驗(yàn)證互作,還能用于哪些實(shí)驗(yàn),當(dāng)然,關(guān)子應(yīng)該是賣不了了,畢竟標(biāo)題已經(jīng)出賣了我的想法。
那燈籠的使用主要有兩個主要組成部分,燈籠罩和一個亮度可觀的光源,但是只有這兩個就可以讓一個燈籠發(fā)揮照明的作用嘛,很明顯是不可以的。因?yàn)楣庠词切枰稽c(diǎn)亮的,不管是古時的紙燈籠使用火折子點(diǎn)亮還是現(xiàn)代的手電tong亦或者是科幻電影中的賽博手電或者核能手電,都避免不了需要點(diǎn)亮這一步。結(jié)合上面提到的關(guān)于燈籠的幾個特點(diǎn),我們可以窺見分子燈籠的大體結(jié)構(gòu),當(dāng)然,火折子也是必須的,但這里的火折子不是指熒光素酶的底物,而是熒光素酶本身,底物只是他的能量來源。
2022年,一篇名為“Genetically encoded BRET-activated photodynamic therapy for the treatment of deep-seated tumors”揭示了一類特殊的分子燈籠研究方向。光動力療法(PDT)是基于光誘導(dǎo)光敏劑介導(dǎo)的活性氧類(ROS)的抗癌活性的癌癥治療的最有影響力的方法之一,但是有限的光穿透組織的深度不能治療深層腫瘤,因此落實(shí)到實(shí)際的臨床應(yīng)用上,依舊有很明顯限制。文章在這里提出了一個依賴BRET激活PDT的概念,構(gòu)建一個表達(dá)內(nèi)部光源以及結(jié)合光敏劑(PS)的體系,依賴于熒光素酶本身的強(qiáng)穿透性以及本身不需要光照僅靠底物酶促反應(yīng)可以發(fā)光的特性,其可以遞送到位于幾乎無限深度的腫瘤,且這個治療可以通過注射底物進(jìn)行控制。為了展示這個體系,研究人員設(shè)計(jì)了遺傳nanoluc-miniSOG的BRET對,其中中nanoluc作為光源的供體,光毒性蛋白miniSOG作為受體接受并發(fā)出熒光,在注射底物后,在nanoluc的激活下產(chǎn)生ROS。
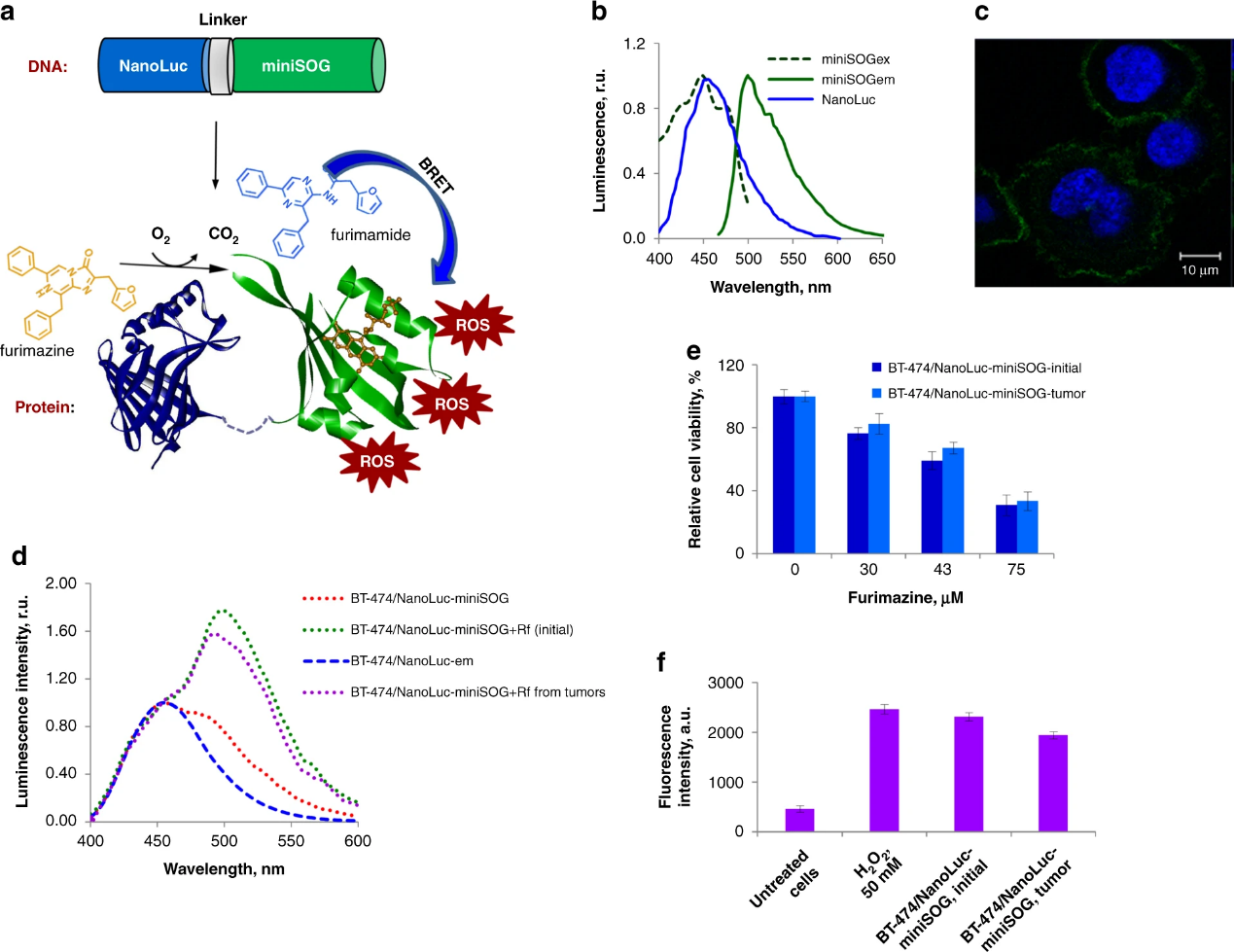
圖1: nanoluc-miniSOG體系示意圖及細(xì)胞實(shí)驗(yàn)效果展示【1】
后續(xù)為了驗(yàn)證在動物體內(nèi)該系統(tǒng)是否依舊可以發(fā)揮功能,研究人員將穩(wěn)定表達(dá)nanoluc-miniSOG的BT-474細(xì)胞注射到小鼠體內(nèi)進(jìn)行成瘤,在腫瘤生長到預(yù)期大小之后,對成瘤的小鼠進(jìn)行不同的處理,結(jié)果顯示該體系對于腫瘤的抑制具有顯著效果。
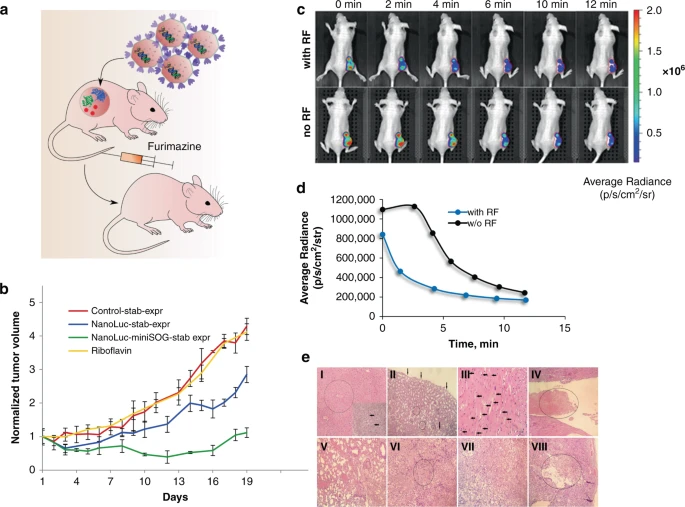
圖2:不同處理的成瘤小鼠腫瘤變化情況【1】
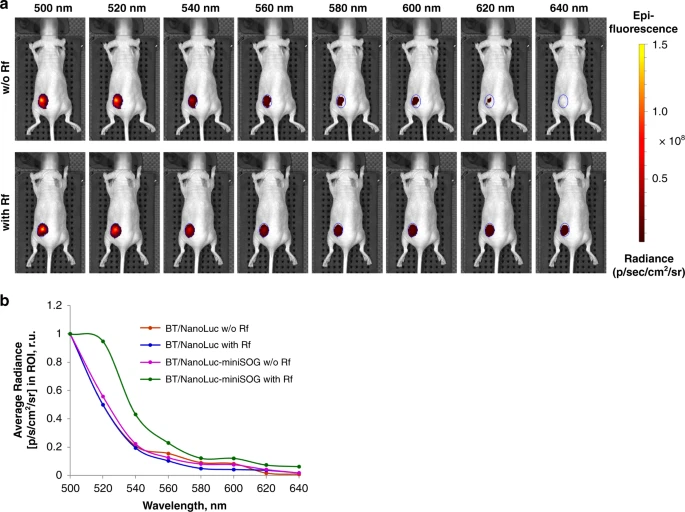
圖3:直接檢測NanoLuc-miniSOG荷瘤小鼠中離子化miniSOG的熒光信號【1】
最后為了驗(yàn)證攜帶NanoLuc-miniSOG的假病毒載體直接注射對于腫瘤生長的影響,研究人員使用帶有her2特異性支架蛋白DARPin_9-2931假型的慢病毒載體,將nanolucminisog遺傳構(gòu)建體傳遞到動物模型中的BT-474腫瘤中(圖4a)。為此,在截?cái)嗦檎畈《?MV)的糖蛋白(血凝素HcΔ18和融合蛋白FcΔ30)存在的情況下,制備了人類免疫缺陷病毒HIV-1載體顆粒,并用DARPin9_29修飾MV血凝素蛋白的c端,使其對自然識別的CD46受體的趨向性改變?yōu)镠ER2受體。DARPins(設(shè)計(jì)的錨蛋白重復(fù)序列蛋白)是一種非免疫球蛋白性質(zhì)的結(jié)合支架,已被開發(fā)為免疫球蛋白蛋白的替代品)
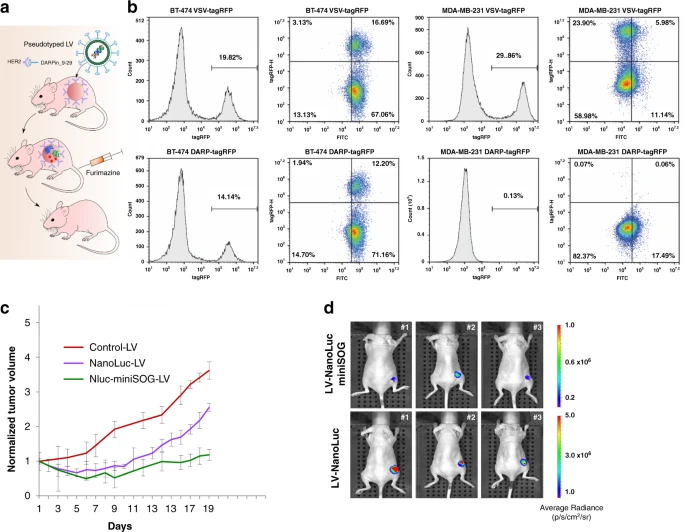
圖4: 以HER2陽性腫瘤為靶向?qū)ο蟮腘anoLuc-miniSOG病毒的干預(yù)效果【1】
結(jié)果而言,效果顯著,不管是腫瘤細(xì)胞中還是對于一定大小的瘤體都有較好的殺傷效果,結(jié)合底物的使用,還可以做到特定階段對于藥物的殺傷,通過一個可以被控制的開關(guān),打開深層組織臟器腫瘤殺傷的新方向。
參考文獻(xiàn)…
1. Genetically encoded BRET-activated photodynamic therapy for the treatment of deep-seated tumors
