在生物制藥下游生產工藝中,色譜層析技術應用已逐漸成為不可或缺的一部分,其在提高產品純度、除雜有效性和病毒去除等方面發揮著不可替代的作用。層析填料作為其核心關鍵物料,其性能直接影響產品的安全性和有效性,而做好填料保存研究正是確保填料在儲存期間維持穩定性能的關鍵環節。
填料保存研究的意義
填料保存研究的目的在于確認填料在當前儲存條件下的穩定性,為填料的儲存條件、有效期和復驗期的制定提供科學依據。如果填料沒有進行適當的保存研究,可能會導致填料性能下降,甚至影響純化效果,對藥品質量產生挑戰,甚至影響藥品的安全性和有效性,最終造成生產成本的增加。
填料保存研究的法規要求
填料保存研究沒有統一的法規標準,但由于其會直接影響填料的壽命,多個法規和指南提出了相關要求,其核心是,填料保存研究必須確保填料在整個使用期間性能穩定,不影響藥品質量。具體的法規要求可以參考填料壽命研究相關的法規:
Table 1. 層析填料壽命研究(含保存研究)的法規指南要求

供應商進行的填料保質期研究
各供應商按其SOP的要求進行填料的保質期研究,常規做法如表所示:
Table 2. 供應商常規的填料保存研究的做法

藥企進行的填料保存研究
盡管層析填料的供應商可以提供填料的保存時限、保存液的抑菌效果等數據,但是藥企仍需開展相關層析填料保存驗證工作。主要是由于供應商提供的層析填料保存數據是使用新鮮填料,并且在散裝保存條件下進行。大多數生物制藥的實際生產中,保存的層析填料往往是使用過的,而且很多時候是柱上保存。層析填料的保存驗證應當考慮到這些實際條件。早期的填料保存研究相對簡單,多依賴于供應商的建議和用戶經驗。隨著制藥行業的發展,尤其是GMP要求的不斷提高,填料保存研究逐漸系統化和科學化。
Table 3展示了一個層析填料保存驗證的可操作性示例。
Table 3. 層析填料保存驗證的示例
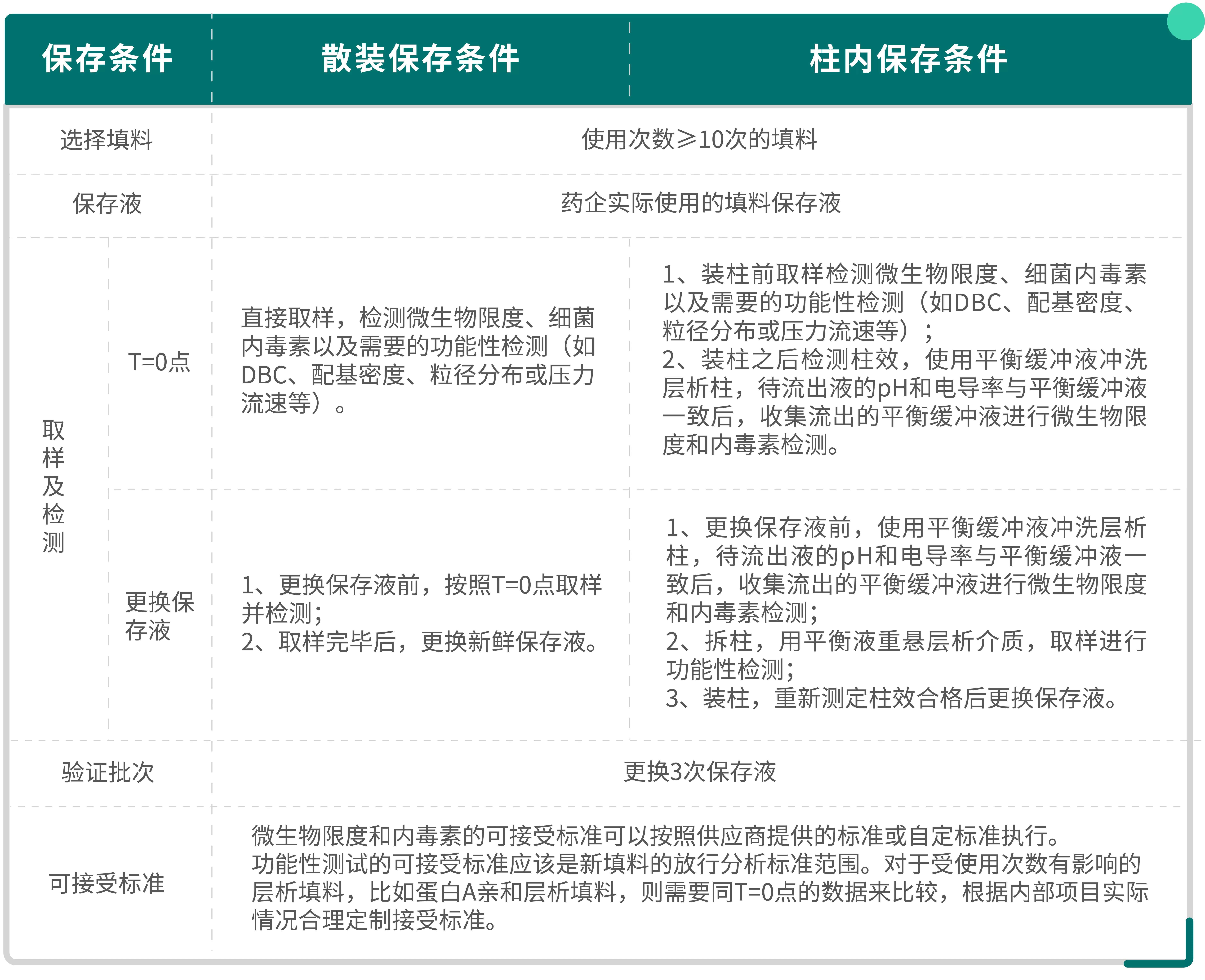
盡管當前不同企業和供應商對填料保存的具體做法可能有所不同,但行業內已形成一些基本共識:
• 填料的保存策略應基于科學研究和實驗數據,而非主觀判斷;
• 在進行填料保存研究,需要跨部門(包括研發、生產和質量管理部門等)協作;
• 應明確填料的保存驗證是工藝驗證生命周期的一部分,且需要在使用過程中不斷確認和優化。
填料保存研究的注意事項
進行填料保存研究時,需注意以下關鍵點:
• 填料保存研究應在代表實際儲存條件(包括溫度、濕度、光照等)的環境下進行;
• 應根據填料的特性,保存條件(散裝和/或柱上保存),歷史數據確定合理的取樣測試頻率;
• 制定科學合理的可接受標準標準;
• 有詳細的文件記錄(包括保存研究的方案、數據和結果等),為監管提交提供證據;
• 填料保存研究過程中,任何保存條件的變更都應通過正式的變更控制程序進行評估和批準。
參考文獻
[1]2025 版《中國藥典》三部“人用重組單克隆抗體制品總論”
[2]FDA “Guidance for Industry:Process Validation: General Principles and Practices”
[3]EMA “CPMP Position Statement on DNA and Host Cell Proteins (HCP) Impurities, Routine Testing Versus Validation Studies,” CPMP/BWP/382/97
[4]PDA Technical Report No.60-3: Process validation: A lifecycle approach Annex 2: biopharmaceutical drug substances manufacturing. Parenteral Drug Association: 2021
