
膽囊切除術后的腹瀉 (PCD) 是膽囊切除術后非常常見的并發癥,其發生率高達 57.2%。現如今由于膽囊結石患病率的增加,以及膽囊切除術作為膽結石患者治療方案,使得PCD在全球范圍內影響著大量人群的健康問題。目前對于PCD發病機制的深刻理解和有效的治療方案仍不清晰。現有研究發現PCD患者腸道菌群存在差異,并且膽囊切除術對腸道菌群的影響也有相關報道。然而,PCD患者腸道菌群的改變僅是腹瀉本身的結果還是PCD發生的促成因素仍沒有定論。此外,腸道菌群變化如何以及在多大程度上導致PCD仍待解開。
2023年2月,來自復旦大學附屬閔行醫院張紫平教授團隊和王立順研究員團隊在Gut Microbes(IF 9.434)上共同發表題為“Gut microbiota alteration after cholecystectomy contributes to post-cholecystectomy diarrhea via bile acids stimulating colonic serotonin”的文章。該研究通過糞菌移植膽囊切除術后腹瀉 (PCD)患者腸道菌群,確定菌群對腹瀉的影響。隨后通過菌群結構功能分析揭示了色氨酸代謝途徑中血清素的重要作用,結合代謝組學發現菌群產生的次級膽汁酸可在體內外刺激血清素產生,并通過TGR5 / TRPA1信號通路介導,最終建立腸道菌群-糞便BAs代謝物-TGR5/TRPA1-血清素軸并明確其在PCD過程中的關鍵作用機制。中科新生命提供了靶向色氨酸代謝組學檢測服務。

研究材料
糞便、血清、結腸組織、細胞系
臨床樣本:膽囊切除術后腹瀉(PCD)患者(n=10),非PCD患者(n=5),健康對照組(HC,n=5);動物模型:抗生素處理的無菌鼠;細胞模型:大鼠胰島腫瘤細胞系RIN14B
技術路線
步驟1:16S rRNA測序揭示腸道菌群及其影響的代謝過程在膽囊切除術后腹瀉(PCD)發生中的關鍵作用;步驟2:靶向代謝組揭示PCD小鼠結腸中血清素的生物合成是其產生不良表型的關鍵因素;
步驟3:PCD腸道菌群通過影響血清素的生物合成及其受體5-HTRs驅動腸道過度蠕動;
步驟4:靶向代謝組再次揭示腸道菌群來源的次級膽汁酸可以刺激血清素的產生;
步驟5:阻斷BAs偶聯的TGR5/TRPA1受體信號通路可以顯著減輕PCD。
研究結果
1. 16S測序揭示腸道菌群及其影響的代謝過程在膽囊切除術后腹瀉(PCD)發生中的關鍵作用研究團隊選擇了20例臨床糞便樣本進行16S rRNA測序,其中包括膽囊切除術后腹瀉(PCD)患者(n=10),非PCD患者(n=5),以及健康對照組(HC,n=5)。α-多樣性分析顯示,與 HC 和 NonPCD 患者相比,PCD患者的菌群豐度及菌群多樣性顯著降低,PCoA以及NMDS也展示了不同樣本組別之間微生物分布與結構的差異。接下來通過糞菌移植實驗構建了基于微生物組的人源化小鼠模型,證實了PCD患者腸道菌群的改變導致了腹瀉的發生,并明確了結腸作為其發生相關生理過程的主要場所。
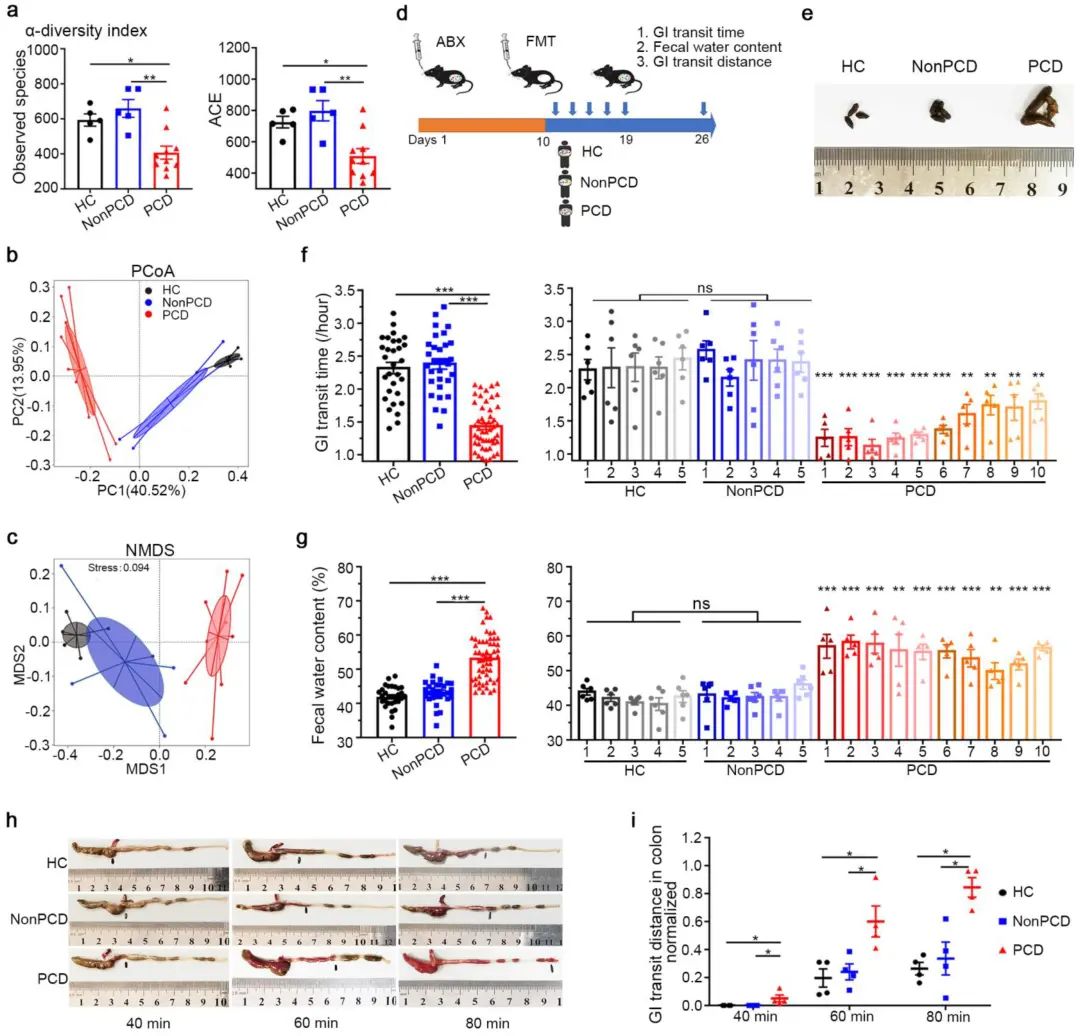
圖1 無菌小鼠在移植PCD腸道菌群后表現出腹瀉表型
為了進一步探索微生物組的功能,作者對人源化模型鼠結腸腔內容物中的菌群進行了著重分析。結果顯示,與NonPCD 和 HC 小鼠相比,PCD小鼠擁有最少的OUT,并且微生物多樣性同樣顯著降低,菌群結構產生了巨大的變化。此外作者也通過PICRUSt 和 Tax4Fun兩款微生物宏基因功能預測工具,分析出色氨酸代謝途徑的變化可能是PCD小鼠發生腹瀉的潛在影響因素。
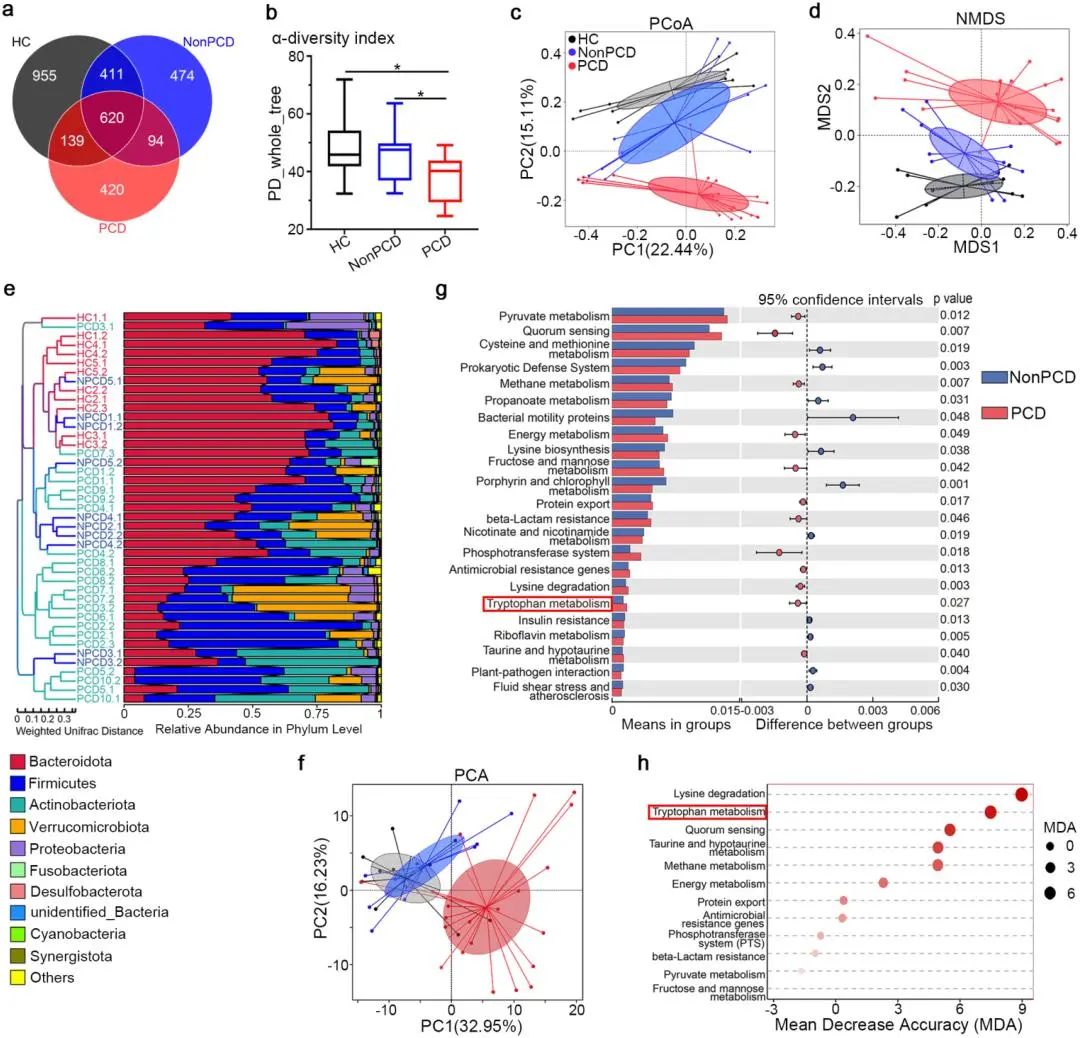
圖2 色氨酸代謝在PCD小鼠結腸內容物的宏基因組功能預測中顯著富集
2. 靶向代謝組揭示PCD小鼠結腸中血清素的生物合成是其產生不良表型的關鍵因素
由于血清素(5-羥色胺)是色氨酸的基本代謝物,通常參與刺激腸道蠕動的調節。所以作者首先通過靶向代謝組學技術量化了其在三組小鼠結腸和血清中的表達水平。結果顯示,與 HC 和 NonPCD 相比,PCD小鼠結腸和血清中的血清素水平大約升高一倍,并且與腸胃道傳輸時間呈負相關。為了明確血清素的來源,作者也通過免疫組化等實驗確認血清素水平的升高并非來源于腸道嗜鉻細胞(血清素的主要合成細胞)的過度增殖,而是可能源于其在PCD小鼠結腸中的過量產生。后續的分子實驗也進一步證明了上皮細胞中血清素受體 5-HT3R 和 5-HT4R過度表達介導的結腸血清素升高,可能是加速PCD小鼠結腸蠕動的關鍵驅動因素。

圖3 PCD腸道菌群導致小鼠結腸中血清素水平升高和其受體5-HTRs的過度表達
3. PCD 腸道菌群通過影響血清素的生物合成及其受體5-HTRs驅動腸道過度蠕動
為了進一步證實血清素及其受體5-HTRs是PCD小鼠腸道加速蠕動的關鍵因素,作者進行了相關驗證實驗。結果顯示,使用色氨酸羥化酶1抑制劑降低結腸中血清素的水平,以及通過血清素受體選擇性拮抗劑阻斷其與血清素的結合,可以顯著改善PCD小鼠腹瀉表型。這些結果證實了累積的血清素對結腸過度蠕動的影響,并證明了血清素受體5-HTRs的特異性阻斷對 PCD 小鼠的治療作用。

圖4 抑制血清素的合成和選擇性阻斷血清素受體5-HTRs可顯著改善PCD小鼠的腹瀉表型
為了確定腸道菌群對血清素合成的具體影響,作者在細胞層面進行了驗證實驗。分別將清洗過的腸道菌群與過濾掉菌群后的糞便溶液糞與RIN14B 細胞系共同孵育,結果顯示腸道菌群的代謝物是影響血清素合成的關鍵因素。
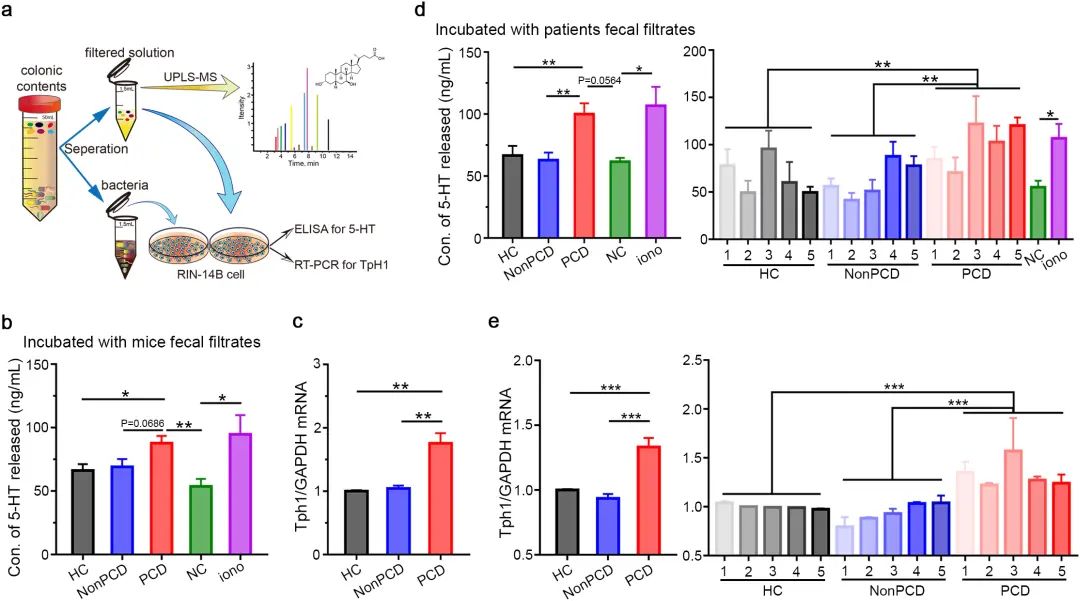
圖5 PCD患者及其人源小鼠的微生物代謝物刺激了RIN14B細胞系中的血清素生物合成
4. 靶向代謝組再次揭示腸道菌群來源的次級膽汁酸可以刺激血清素的產生
之前的研究中作者已經證實了腸道菌群紊亂導致的次級膽汁酸(BAs)代謝改變是PCD的關鍵原因,但是BAs 代謝產物的變化是否通過血清素導致PCD仍然未知。接下來作者通過靶向代謝組分析發現PCD小鼠糞便中的BAs代謝產物表達差異顯著,并在RIN14B細胞系以及模型鼠中進一步確認這些顯著變化的次級BAs對血清素合成的影響,最終體內實驗和體外試驗均證實了微生物來源的次級BAs可以刺激血清素的產生。
為了進一步證實次級BAs誘導 PCD 患者血清素的過量產生,作者分析了糞便膽汁酸代謝和色氨酸代謝。結果顯示與 HC 和非 PCD 相比,PCD 患者糞便中BAs代謝物的表達具有顯著差異,并且KEGG通路富集分析也顯示色胺代謝途徑在 PCD 患者的糞便中明顯富集。進一步結合16sRNA測序分析結果,發現次級BAs的積累可能是由于PCD腸道菌群中過多的BAs代謝菌引起的,如梭狀芽孢桿菌以及為鑒定的Lachnospiraceae。

圖6 微生物來源的次級膽汁酸誘導血清素的過量產生
5. 阻斷BAs偶聯的TGR5/TRPA1受體信號通路可以顯著減輕PCD
部分次級膽汁酸,如DCA、LCA和HDCA被發現是G蛋白偶聯膽汁酸受體1 (GPBAR1) 或 TGR5的特異性激動劑,瞬時受體電位錨蛋白1 (TRPA1) 可使腸嗜鉻細胞在TGR5激活后分泌血清素以調節腸胃運動。因此,作者為了驗證菌群BAs代謝產物在PCD中的腹瀉誘導作用,通過SBI-115和HC-030031兩種選擇性阻斷劑阻斷了這兩種受體,通過免疫熒光實驗結合腹瀉相關表型實驗,證實了微生物來源的次級BAs在PCD中過度促進腸道蠕動的作用,并提示了TGR5 拮抗劑和 TRPA1 抑制劑對 PCD 的潛在治療功效。

圖7 PCD腸道菌群通過TGR5/TRPA1信號通路誘發腹瀉
文章小結
該研究證實了腸道菌群的改變影響PCD發生的因果關系,并揭示了該過程中的腸道菌群-糞便BAs代謝物-TGR5/TRPA1-血清素軸。因此減少腸道血清素的產生或阻斷血清素受體可能是治療PCD的新方式。此外阻斷BAs偶聯的TGR5/TRPA1受體信號通路可以顯著減輕PCD,提示了TGR5拮抗劑和 TRPA1抑制劑對 PCD的潛在治療功效。