2013年,Broad研究所的張峰和Eric S. Lander兩個研究團隊,同時在Science中發表了CRISPR-Cas9的文庫應用,首次把這項技術暴露在了公眾視野中。隨著科研軟實力和CRISPR-Cas9體系開放性的不斷增加,在2017年后文庫篩選已經成為了一種主要的差異基因發掘工具。但是目前仍然有很多人不知道文庫的具體的實驗方式及應用場景。
2022年3月25日,Julia Joung等人在Nature Communications發表“CRISPR activation screen identifies BCL-2 proteins and B3GNT2 as drivers of cancer resistance to T cell-mediated cytotoxicity”,文中借助CRISPR-Cas9文庫篩選技術開展腫瘤研究。本文以此為例,分析CRISPR-Cas9文庫的研究思路。

1 技術思路
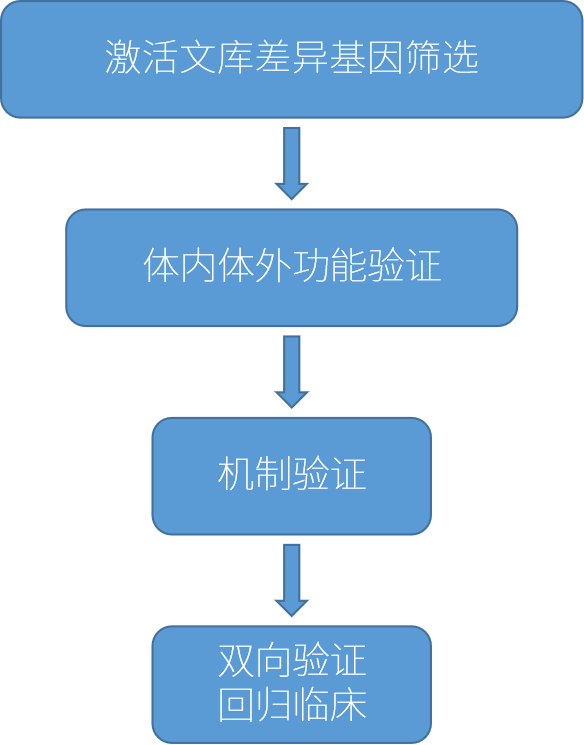
(1)通過CRISPR-Cas9激活文庫確定惡性黑色素瘤細胞A375中與免疫耐受相關的相關基因,并通過MAGeCK與現有轉錄組數據和TCGA數據庫結果分析后,確定4個候選基因,為CD274、MCL1、JUNB、B3GNT2。(差異基因篩選)
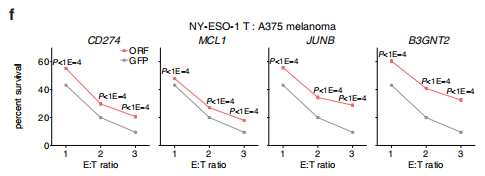
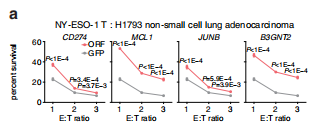
(2)首先,分別構建CD274、MCL1、JUNB、B3GNT2 4個基因的過表達細胞株。然后在體外,通過CTG法(CellTiter-Glo)檢測NY-ESO-1 CAR-T細胞對4株過表達細胞及對照細胞的殺傷能力差異。在體內,使用NGS小鼠皮下移植瘤模型,證明4株過表達細胞及對照細胞對于尾靜脈過繼NY-ESO-1 CAR-T細胞的響應性差異。(基因表型驗證)
(3)通過Caspase-8活性檢測、流式檢測、CHIP-seq及RNA-seq等方法,證明MCL1和JUNB基因通過影響線粒體凋亡信號通路去抵抗FasL和TRAIL誘導的細胞死亡。(機制證明)
(4)通過細胞因子分泌檢測及COIP等實驗證明B3GNT2基因主要通過影響腫瘤細胞與T細胞的受體配體結合發揮免疫耐受功能。(機制證明)
(5)構建4個差異基因敲低腫瘤細胞株,反向驗證是否有免疫增敏效果。同時用小分子抑制劑證明基因正確性。(多向驗證)
2 研究內容
作者通過首先制備CRISPR-Cas9激活文庫,然后構建NY-ESO-1抗原高表達的文庫細胞株,繼而與NY-ESO-1的CAR-T細胞進行共培養,通過瞬時殺傷和長效殺傷的兩種篩選方式進行篩選,將篩選后的樣本通過CRISPR-Screen進行差異基因初步篩選。在篩選好的差異基因與公共數據庫中的數據進行比對后,確定明顯差異表達的CD274、MCL1、JUNB、B3GNT2 4個基因進行后續研究。
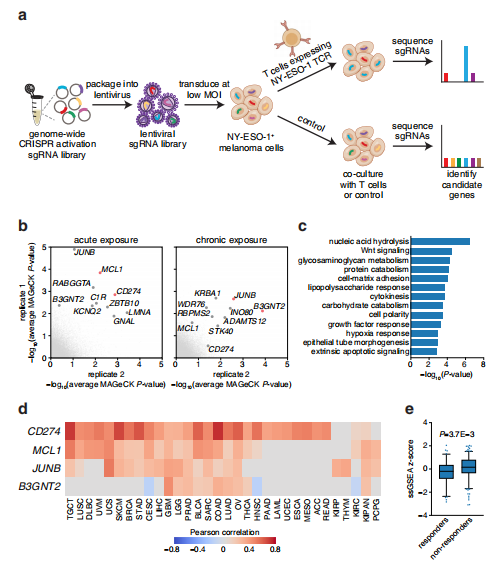
TIP1:好的開始是成功的一半啊,集美們,一定要用新穎的技術,結合已有的公共數據庫數據進行聯合的基因發掘工作啊。
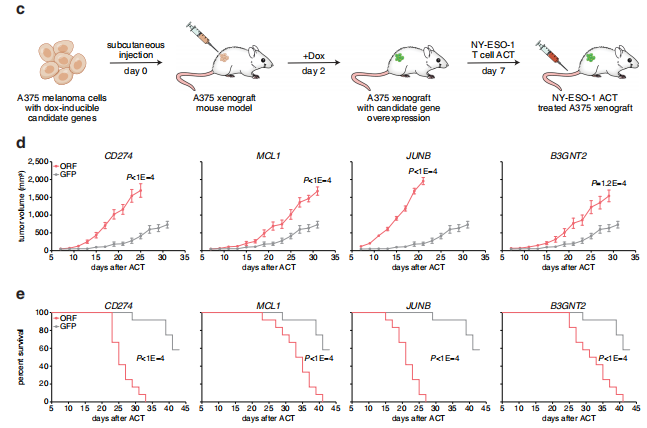
基于表達NY-ESO-1抗原的人黑色素瘤細胞A375構建CD274、MCL1、JUNB、B3GNT2基因過表達腫瘤細胞,在體外與NY-ESO-1 CAR-T細胞共培養,后用CTG法檢測各個過表達細胞株與對照細胞株的存活細胞之差,證明4個基因過表達后會降低CAR-T細胞的殺傷活力。
步驟2中的過表達和對照構建NGS小鼠,皮下腫瘤模型,成瘤后尾靜脈過繼CAR-T細胞,實驗證明,過表達腫瘤對CAR-T細胞的治療響應性更差,小鼠生存期更短。
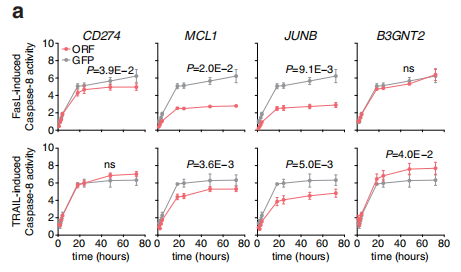
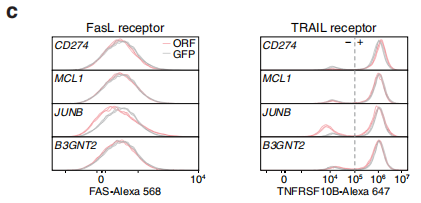
已有研究表明,JUNB是一種轉錄因子,并且能夠影響NKG2D配體,從而影響NK細胞的正常殺傷功能,而MCL1更是在早期的研究中就發現與FASL和TRAIL受體功能相關,因此作者也受其思路啟發,從受體方面入手驗證。過表達和對照用流式檢測FASL和TRAIL受體的表達量,確定過表達JUNB和MCL1后,會影響受體表達;JUNB和MCL1過表達細胞用 FasL 或TRAIL處理后,檢測Caspase-8的活性,發現JUNB的作用會被扭轉,因此也確認JUNB是通路下游非常重要的一環;隨后通過CHIP-seq和RNA-seq兩種技術,證明JUNB直接調控的基因是NFKB,并且能夠通過操控NFKB來影響下游信號通路的轉導,至此,完美解釋了JUNB基因影響免疫耐受的環路,而MCL1并不影響前端的受體表達,因此作者證明它是直接調控了線粒體凋亡相關的BAX和BAK發揮功能。
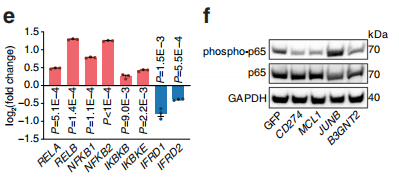
TIP2:再次證明,多讀文章有多重要啊集美們,不要光是天天買買買,一定要看文獻啊,當我們的實驗有了系統的理論基礎和支持,才有了攀登高分文章階梯的登山杖。
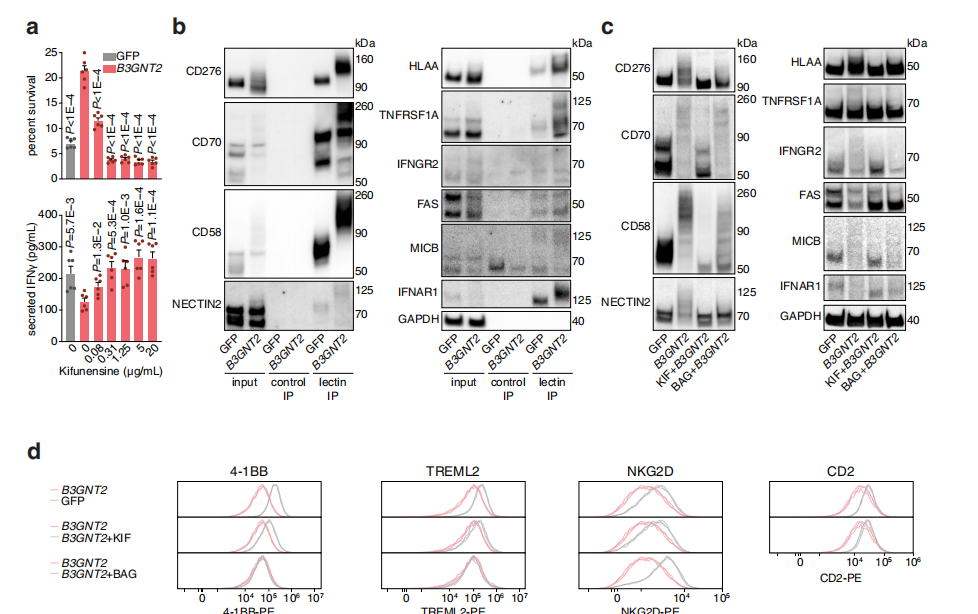
至于B3GNT2基因,目前已知它可以編碼β-1,3-N-乙酰氨基葡萄糖轉移酶 ,因此作者合理推測此基因影響多聚乳糖胺合成,并且目前已經有其他研究結果隱約指明了這一證據。作者在補充實驗中已經通過番茄凝集素檢測實驗證實B3GNT2過表達細胞胞內和胞外中多聚乳糖胺含量都有所增加,而這一現象,是由于B3GNT2誘導的N-糖基化修飾和O-糖基化修飾有關。作者以此作為起點,通過細胞因子分泌實驗和CTG細胞活力證明,在傳統的共培養體系中,持續加入N-糖基化修飾抑制劑KIF,能夠扭轉B3GNT2過表達帶來的免疫耐受;通過COIP實驗B3GNT2過表達之后番茄凝集素對于各類腫瘤細胞表面受體結合能力大幅提升,這也支持了作者的假說。
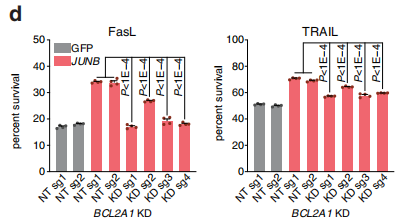
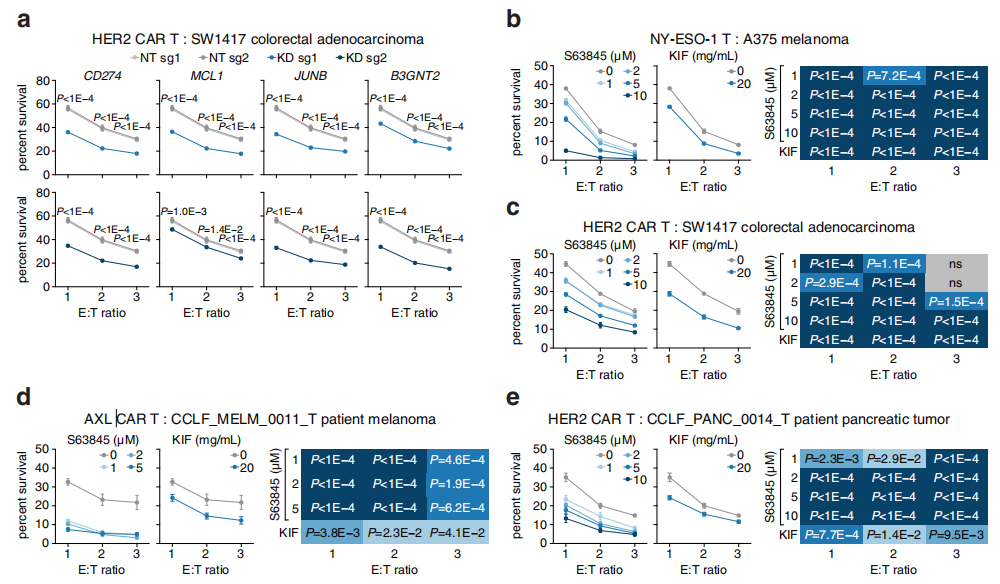
最后當然多項驗證了,首先作者先在表達HER2抗原的SW1417細胞中敲低CD274、MCL1、JUNB、B3GNT2 這4個基因,然后通過與HER2 CAR-T細胞共培養驗證基因的有效性和廣泛性,后續在多種腫瘤細胞中證實N糖基化修飾抑制劑KIF和MCL1小分子抑制劑S63845的功能,從另一角度證明了基因功能,并且為臨床應用打開思路。
?
TIP3:強調一點,對于腫瘤研究來說,盡量一定要回歸臨床,當我們的研究有了一定的臨床指導意義,我們才好發文章啊。
綜上所述,這篇文章系統的向我們展示了,如何用CRISPR-Cas9文庫發掘差異基因及后續實驗驗證的全套過程。文章涵蓋了文庫篩選及腫瘤免疫兩個領域內研究熱點,在選題方面可以說是羚羊掛角,不負高分期刊之名,值得我們深入學習和參考。