元素雜質 elemental impurities
元素雜質有多種來源,合成工藝中金屬催化劑的殘留、原輔料的引入、生產設備和包裝等接觸材料帶入等,均與藥品質量研究密切相關。
國際人用藥物注冊技術協調會議(ICH)于2013年發布《Q3D元素雜質指導原則》,并進行多次修訂,對元素雜質的分類、風險、每日允許暴露量(PDE)、限度和控制策略等進行了詳細評估,旨在為藥品中元素雜質的定性和定量控制提供指導方針。
本文將分享一些元素雜質檢測項目拋磚引玉,與醫藥檢測領域伙伴共同探索藥物中的元素雜質研究。
案例分享 elemental impurities
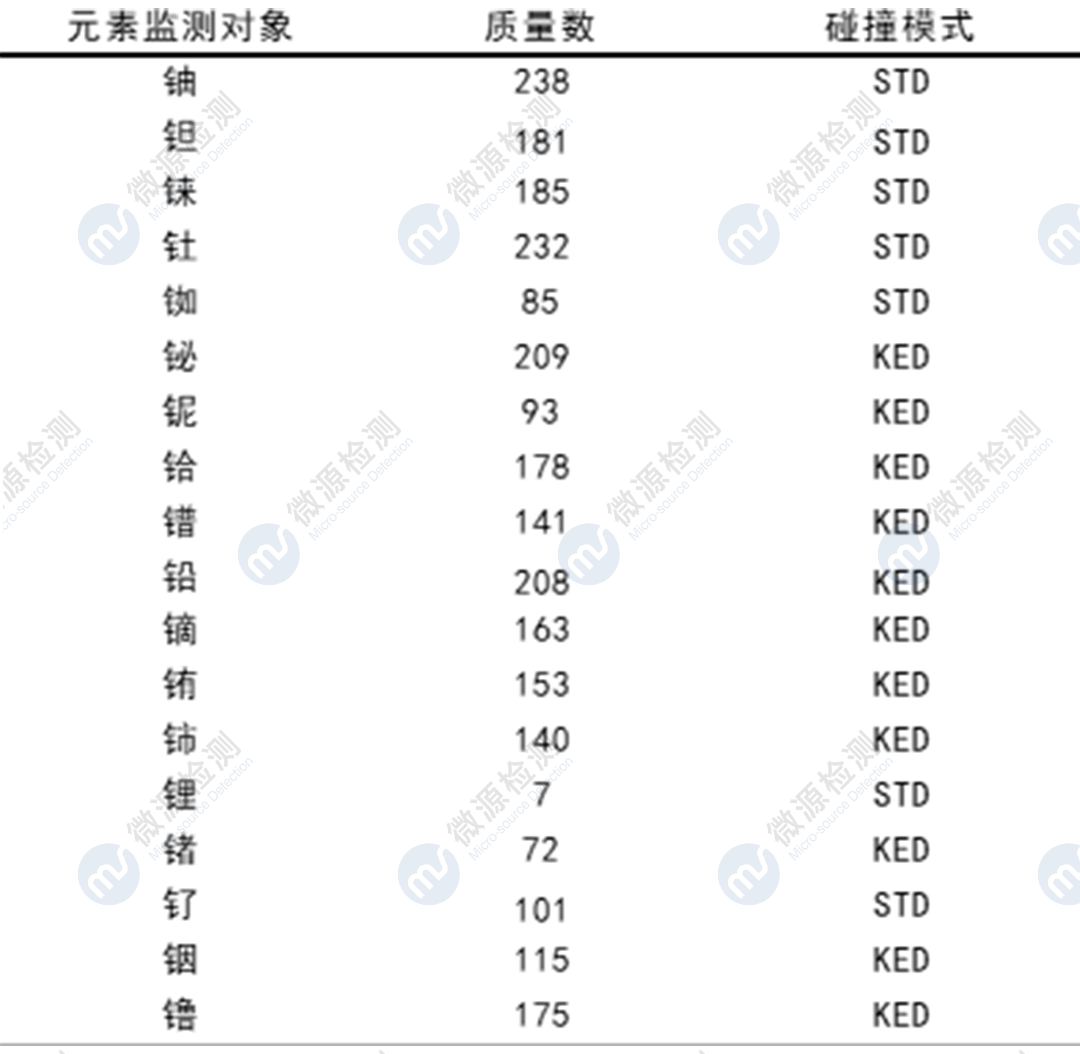
Ⅰ.利用ICP-MS對某原料藥中13種元素(鈾U、鉭Ta、錸Re、釷Th、銣Rh、鉍Bi、鈮Nb、鉿Hf、鐠Pr、鉛Pb、鏑Dy、銪Eu、鈰Ce)進行了方法學開發與驗證,系統適用性、專屬性、靈敏度、線性、準確度、精密度、溶液穩定性等驗證指標均符合可接受標準,檢測結果中各元素雜質殘留量均符合限度要求,幫助委托方完成該品種的元素雜質風險評估。


Ⅱ .利用ICP-OES對某原料藥中2個元素(碘I、硅Si)進行了方法學開發與驗證,系統適用性、專屬性、靈敏度、線性、準確度、精密度、溶液穩定性等驗證指標均符合可接受標準,檢測結果中各元素雜質殘留量均符合限度要求,幫助委托方完成該品種的元素雜質風險評估。

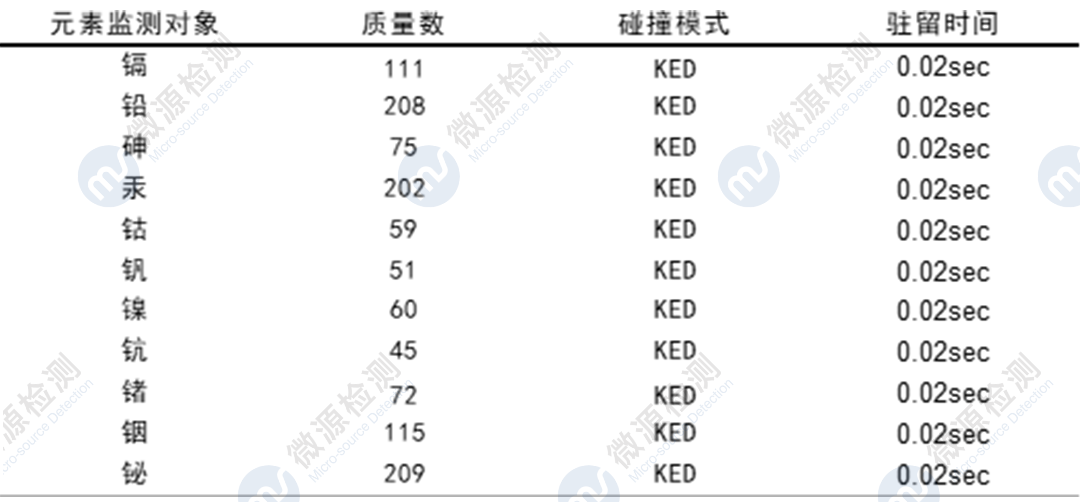
Ⅲ 利用ICP-MS對某創新藥中7個元素(鎘Cd、鉛Pb、砷As、汞Hg、鈷Co、釩V、鎳Ni)進行了方法學開發與驗證,系統適用性、專屬性、靈敏度、線性、準確度、精密度、溶液穩定性等驗證指標均符合可接受標準,檢測結果中各元素雜質殘留量均符合限度要求,幫助委托方完成該品種的元素雜質風險評估。


項目經驗 elemental impurities
√ 口服藥物中常規7種元素雜質檢測、注射藥物中常規10種元素雜質檢測、吸入藥物中常規14種元素雜質檢測、質量工藝添加等其他高風險元素的檢測;
√ 可根據不同測試需求,進行特殊限度的元素檢測,滿足低限度的方法學開發和方法學驗證。根據客戶需求及不同檢測目的,滿足境內外多體系藥物注冊申報研究要求并支持審計等……
指導原則 elemental impurities
? ICH Q3D
? USP <232>
? USP <1225>
? Ch.P四部指導原則
? Ch.P四部通則0411
? Ch.P四部通則0411
? Ch.P四部通則2321
文末總結 elemental impurities
實驗室根據各元素性質和限度進行方法開發(主要進行樣品前處理的方法開發)和驗證,提供快速高靈敏度的結果,確保數據結果的可靠性。代表批次檢測并確定控制策略,已開發出65種元素的分析方法。
嚴格監測和控制元素雜質在藥物制劑中的總量, 分析元素雜質可能引入的途徑來制定控制策略, 如調整相關生產工藝、 選擇合適的容器設備等, 以確保元素雜質水平控制符合限度要求, 為藥品質量監管提供有力保障,微源檢測元素雜質檢測服務能夠滿足境內外多體系藥物注冊申報研究要求,支持客戶審計,配合完成全球各國家或地區藥監部門的現場核查。
