.png?access_token=4e1d74c9-e0ea-45ae-8ff5-b4a3aca90a19)
簡介
作為我們不對稱催化產品組合的一部分,阿拉丁以(R,產品貨號:B120975)和(S,產品貨號:B120963)對映體的形式提供異硫脲有機催化劑苯并四咪唑(HBTM)。這些化合物已廣泛應用于低催化劑負載量的各種官能團的對映選擇性轉化和動力學拆分。

代表性轉化
動力學拆分
S-HBTM最初是由Birman及其同事開發(fā)作為酶促條件的一種替代而用于動力學中仲醇的拆分[1]。已報道了最多有122種不同的可選變量。HBTM催化劑已在各種溫度范圍內與多種有機溶劑一起被用于烯丙基、炔丙基和芐基仲醇的動力學拆分,反應通常在數(shù)小時內完成,在較低溫度(0 - 55 ℃)下的甲苯、氯仿或叔戊醇中可達到最佳條件[1, 2]。
HBTM同樣可用于α-芳基鏈烷酸、α-芳氧基-鏈烷酸、α-烷氧基-鏈烷酸、α-鹵代鏈烷酸和受保護的α-氨基酸的動力學拆分[3, 4]。已報道了最多有96種不同的可選變量。該轉化通常是在低溫下利用甲苯作為溶劑進行24小時反應來完成的。
同樣,有學者研究了利用HBTM對對映體富集的α-硫代鏈烷酸的形成進行了動態(tài)動力學拆分[4, 5]。該過程可選擇多種不同的底物,并且具有高產率和高對映體純度。
對映選擇性轉化
HBTM已被用于惡唑基碳酸酯的不對稱羧基轉移反應[6]。該過程以二氯甲烷作為溶劑,在低溫下反應16小時,底物普適性較好,能以較高的產率和對映選擇性得到相應的產物。

有研究表明HBTM可用于不對稱親核體催化邁克爾-醛醇-β-內酰胺化(NCMAL)的串聯(lián)反應[7]。該過程是在四氫呋喃/二氯甲烷中進行24小時的反應發(fā)生的,從而得到具有高非對映異構體比率、高產率和高對映純度的產物。
絕對構型的測定
HBTM是被選擇用于競爭對映選擇性轉化(CEC)方法的催化劑,該方法可用于分配對映體富集的立體中心的絕對構型。利用HBTM的CEC方法已被報道用于仲醇,其中反應的轉化率是通過1H NMR[8]和TLC進行測量的[9]。TLC分析也已被納入為本科階段的實驗室實驗課程中了[10]。該過程是在室溫下進行的,需經(jīng)歷30分鐘至數(shù)小時不等。
以下助記符可用于識別使用R-HBTM和S-HBTM催化劑的仲醇的絕對構型[8-10]。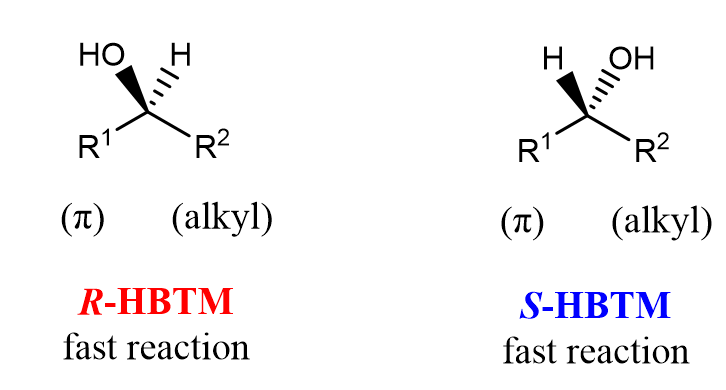
利用HBTM的CEC方法已被報道用于確定惡唑烷酮、內酰胺和硫內酰胺的絕對構型[11]。該過程通常是在室溫或50 oC條件下進行數(shù)小時后完成的。以下助記符可用于識別這些使用R-HBTM和S-HBTM催化劑的體系的絕對構型。
更多研究
HBTM的親核性和Lewis堿度已通過來自利用苯甲醛離子的一系列實驗的速率和平衡常數(shù)而進行了研究[12]。此外,還對HBTM催化的仲醇酯化反應進行了詳細的動力學分析,為該轉化的催化循環(huán)提供了思路和想法[13]。
參考文獻
1. Purification of Basic Compounds with Functionalized SilicaGel. Synfacts. 2008(10): 1115-1115. https://doi.org/10.1055/s-2008-1078198
2. Li X, Jiang H, Uffman EW, Guo L, Zhang Y, Yang X, Birman VB. 2012. Kinetic Resolution of Secondary Alcohols Using Amidine-Based Catalysts. J. Org. Chem.. 77(4): 1722-1737. https://doi.org/10.1021/jo202220x
3. Yang X, Birman V. 2009. Homobenzotetramisole-Catalyzed Kinetic Resolution of α-Aryl-, α-Aryloxy-, and α-Arylthioalkanoic Acids. Adv. Synth. Catal.. 351(14-15): 2301-2304. https://doi.org/10.1002/adsc.200900451
4. Yang X, Birman VB. 2011. Chem.–Eur. J.. 17, 11296.
5. Yang X, Birman VB. 2011. Nonenzymatic Dynamic Kinetic Resolution of α-(Arylthio)- and α-(Alkylthio)alkanoic Acids. Angew. Chem. Int. Ed.. 50(24): 5553-5555. https://doi.org/10.1002/anie.201007860
6. Joannesse C, Johnston C, Concellón C, Simal C, Philp D, Smith A. 2009. Isothiourea-Catalyzed Enantioselective Carboxy Group Transfer. Angewandte Chemie International Edition. 48(47): 8914-8918. https://doi.org/10.1002/anie.200904333
7. Liu G, Shirley ME, Van KN, McFarlin RL, Romo D. 2013. Rapid assembly of complex cyclopentanes employing chiral, α, β-unsaturated acylammonium intermediates. Nature Chem. 5(12): 1049-1057. https://doi.org/10.1038/nchem.1788
8. Wagner AJ, David JG, Rychnovsky SD. 2011. Determination of Absolute Configuration Using Kinetic Resolution Catalysts. Org. Lett.. 13(16): 4470-4473. https://doi.org/10.1021/ol201902y
9. Wagner AJ, Rychnovsky SD. 2013. Determination of Absolute Configuration of Secondary Alcohols Using Thin-Layer Chromatography. J. Org. Chem.. 78(9): 4594-4598. https://doi.org/10.1021/jo400432q
10. Wagner AJ, Miller SM, Nguyen S, Lee GY, Rychnovsky SD, Link RD. 2013. J. Chem. Educ. in press..
11. Perry MA, Trinidad JV, Rychnovsky SD. 2013. Absolute Configuration of Lactams and Oxazolidinones Using Kinetic Resolution Catalysts. Org. Lett.. 15(3): 472-475. https://doi.org/10.1021/ol303239t
12. Maji B, Joannesse C, Nigst TA, Smith AD, Mayr H. 2011. Nucleophilicities and Lewis Basicities of Isothiourea Derivatives. J. Org. Chem.. 76(12): 5104-5112. https://doi.org/10.1021/jo200803x
13. Wagner AJ, Rychnovsky SD. 2013. Kinetic Analysis of the HBTM-Catalyzed Esterification of an Enantiopure Secondary Alcohol. Org. Lett.. 15(21): 5504-5507. https://doi.org/10.1021/ol402643n
阿拉丁提供相關產品,詳情可查看:Homobenzotetramisole (HBTM): A General Organocatalyst for Asymmetric Acylations (aladdin-e.com)
